仿制药一致性评价之后 中药注射剂也将启动再评价工作
仿制药一致性评价之后,中药注射剂也将启动再评价工作。
“在中国的市场上仿制药还是临床用药的主体,我们要扩大临床试验的资源,探索注射剂质量和疗效一致性评价的方法,要启动中药注射剂药品安全性、有效性的再评价工作。”国家食品药品监督管理总局局长毕井泉在2月27日国新办发布会上表示。
2015年,我国启动了仿制药一致性评价,目前仿制药一致性评价办公室已经接到参比制剂备案申请4000多件,备案品种700多个。
已经启动的仿制药一致性评价的临床试验还仅限于口服固体制剂,那么注射剂的一致性评价的临床试验如何做,将是注射液一致性评价的关键。
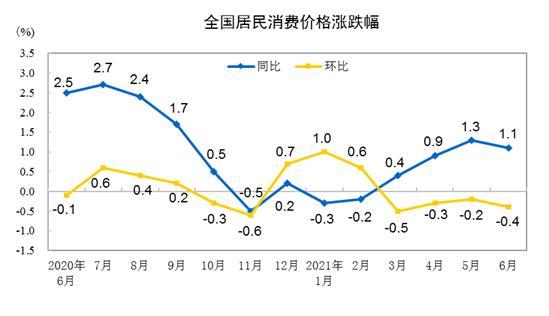
据2015年《国家药品不良反应监测年度报告》中描述,按药品剂型统计,2015年药品不良反应/事件报告涉及的药品剂型分布中,注射剂占61.3%、口服制剂占34.7%、其他制剂占4.0%。注射剂所占比例较2014年增加3.5%,口服制剂比例降低1.5%。
2015年全国药品不良反应监测网络共收到中药注射剂报告12.7万例次,其中严重报告9,798例次(7.7%).2015年中药不良反应/事件报告中,注射剂占比例为51.3%,与2014年相比降低2.1%。
其中,中药注射剂严重报告主要涉及全身性损害、呼吸系统损害、皮肤及其附件损害等,包括过敏样反应、过敏性休克、寒战、发热、呼吸困难、胸闷、心悸、瘙痒、皮疹、恶心、呕吐等表现,与往年监测情况基本一致。
2015年中药注射剂报告数量排名居前的类别是理血剂、补益剂、开窍剂、清热剂、解表剂、祛痰剂,共占中药注射剂报告的97.0%。报告数量排名前五名的药品分别是:清开灵注射剂、参麦注射剂、血塞通注射剂、双黄连注射剂、舒血宁注射剂。
此外,2015年中药注射剂总体报告排名前20位药品(占全年中药注射剂报告87.6%)合并用药情况进行分析,其总体报告涉及合并用药占43.4%,严重报告涉及合并用药占56.5%
透过这些数字分析,可见启动注射剂的质量和疗效一致性评价,存在其必要性。
毕井泉表示,“过去我们批准上市的药品没有与原研药质量疗效一致性的要求,不是强制性的要求,所以有些药品在疗效上与原研药存在差距。开展仿制药质量疗效一致性评价的目的,就是要使我们生产的仿制药能够在临床上与原研药相互替代。好处是可以减轻社会的医药费负担,可以提高中国药品企业的国际竞争力,这也是促进医药产业供给侧结构性的改革。”
此外,毕井泉表示,要建立药品电子通用技术文档系统(eCTD系统),争取今年年底能够实现按新系统实行电子申报和审评,这样就可以减轻企业,特别是在境外申报的企业,到中国来申报基本上技术要求是一样的,格式是一样的,减轻大家的负担。