多省下调抗癌药价格 最高降幅或达50%
专家称仿制药质量有待提升,药品招标、医保支付等政策需要完善
一段时间来,针对抗癌药的举措不断,已经有部分药企开始下调抗癌药品采购价格,四川省也成为首个公布关于抗癌药专项谈判的省份。对抗癌药生产企业来说,无论是专项谈判还是已经持续近三年的药品价格谈判,能够以价换市场是不少企业的出发点,更重要的是,高质量的仿制药亦有希望入局,进一步拉动价格下调。不过在仿制药层面,一致性评价之后的药品招标、医保支付、医院准入等多方面的配套政策还有待落地。
政策主导
部分抗癌药开始降价
近日,多个省份药采平台陆续传来药品降价的消息。
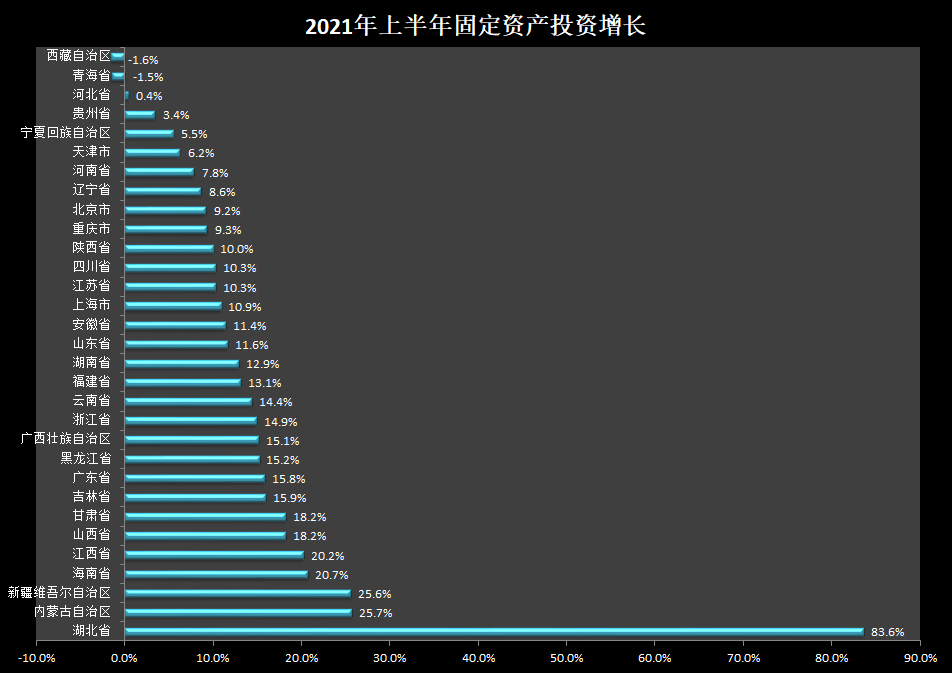
6月29日,湖北省公立医院药品(耗材)供应保障平台发布公告称,响应国家税改政策,根据企业申请,下调辉瑞15个品种、20个品规药品挂网价格,降幅3.4%-10.2%。
7月4日,北京医药集中采购服务中心发布提醒,辉瑞和西安杨森等公司已通过北京市药品阳光采购自主降价功能,其中不乏抗癌药物。以克唑替尼(赛可瑞)为例,该药主要用于治疗非小细胞肺癌,于2011年8月获得美国食药监局优先审批批准上市。原挂网价5.34万元的克唑替尼(250mg规格),每盒将降价2078元,降价幅度为3.9%。
值得注意的是,医保目录外的独家抗癌药,其医保准入谈判也在不断推进中。
7月12日,国家医保局表示,将以省为单位,开展抗癌药专项集中采购。
截至目前,湖北、甘肃、北京、四川、山东等多个省份已开始对抗癌药价格进行调整,四川是首个公布关于抗癌药专项谈判的省份,该谈判已于7月13日启动。
财政部此前公布的103个抗癌制剂清单中,已有82种被纳入医保目录(2017年版)和36个谈判品种,这些品种也将成为抗癌药专项集中采购的重点。在剩余的21个非医保品种中,有17个为独家品种(13个为外企独家,4个为国产独家),这些或将是本次准入谈判的重点。
以往的天价抗癌药有望进入医保目录,患者显然能从中受益。北京肿瘤医院消化肿瘤内科主任医师李燕表示,是否能医保报销是不少肿瘤患者在选择药物时的首要考虑因素,而非疗效。“有些药物,越早使用,能够更好地控制肿瘤,患者的生活质量也会提高。随着使用时间的延后,药物的效价比会降低。”
咨询公司Latitude Health预测,这轮国家意志主导的“操作”,有望使得国家医保目录内的进口抗癌药物价格可能会降低10%,目录外进口抗癌药物可能会降价高达50%,这也是它们被纳入国家医保目录的前提条件。
以价换量
医保准入谈判成关键
2017年4月,人社部确定了纳入2017年国家基本医疗保险、工伤保险和生育保险药品目录谈判范围的44个品种名单。其中,抗肿瘤和免疫调节剂品种数量为22个,成为绝对“主角”。在更早前的2016年国家首批药品价格谈判中,葛兰素史克的慢性乙肝一线治疗药物替诺福韦酯(韦瑞德)、浙江贝达的非小细胞肺癌靶向治疗药物埃克替尼(凯美纳)和阿斯利康的吉非替尼(易瑞沙)3种药物的价格降幅分别达到67%、54%、55%。
进入医保目录,企业当然也有自己的算盘。一位业内人士告诉记者,能否进入医保目录,对药品生产企业和资本市场一直都有重要影响。
以降价换市场,似乎并没有快速显现。以国内知名抗癌药生产企业贝达药业为例,其自主研发的埃克替尼属于国家1类新药,也是中国第一个拥有自主知识产权的小分子靶向抗癌药。埃克替尼进入新版国家基本医保目录后,月均药品费用从12000元降至5500元,降价幅度达54%,销量虽然增长,但贝达药业2017年前三季度营收、净利润同比分别出现了2.42%、34.03%的降幅,但贝达药业则对埃克替尼的市场前景表示乐观。
前述业内人士也表示,能否以降价换市场,也要看竞品进入医保目录的情况,(医保)覆盖范围越广,就越难以降价换市场,在同一个疾病领域,参与谈判的药品种类越多,能够释放的销量红利就越小。
对一些独家品种来说,降价换市场的效果是明显的。2017年7月,罗氏药物赫赛汀被纳入国家医保目录,该药为乳腺癌治疗一线用药,目前没有同成分、同功效的替代品,全国范围内对赫赛汀的用药需求也在短期内出现了激增,今年3月开始,全国多地医院开始出现赫赛汀缺货。罗氏方面称,已经向中国国家药监局申请,将供应中国市场的赫赛汀由现有生产基地转向更高产能的生产基地,以便解决用药荒的问题。
仿制药
多项配套机制待落地
前文提到的36种谈判药品中大多为进口药,在其专利期到期后,国产抗癌仿制药亦有望被纳入到医保药品目录中。通常来说,一种仿制药的价格能够达到原研药的70%,而随着同类仿制药厂家的增多,药品价格还会继续下降,有望达到原研药的30%,甚至更低。以海南双成药业的注射用胸腺法新(免疫调节制剂)为例,该药原研药专利期已过,原研药与双成药业的仿制药也均已通过欧盟审批,两者在质量上并不存在较大差异。进口药在专利期满后售价600元,双成药业的仿制药售价仅为80元,两者相差7.5倍。
仿制药的水平是其中的关键。齐鲁制药集团药物研究院副院长何平曾表示,提高中国仿制药水平和质量是必由之路。我国仿制药存在“粗放式研发和产业化”的问题,质量良莠不齐,低水平重复现象严重;创新药也还处于初级阶段,在基础研究、人才、经验各方面能力都有不足,且对热门领域严重跟风。
2016年2月,国务院办公厅发布的《关于开展仿制药质量和疗效一致性评价的意见》指出,《基本药物目录》(2012年版)中,2007年10月1日前批准上市的化学药品仿制药、口服固体制剂共289个品种,应在2018年底前完成一致性评价。
中国医药企业管理协会会长郭云沛公开表示,开展一致性评价算是一种补课,“只有把这课补好了,才有理由充分说打好了基础。”
在企业层面,一致性评价之后,还面临招标采购等系列环节。海南双成药业股份有限公司董事长王成栋表示,“需要政府完善高质量仿制药招采的配套政策,才能真正把仿制药产业带入良性发展轨道。包括通过一致性评价后的药品招标、医保支付、医院准入等多方面的政策。”
北京大学药学院药事管理与临床药学系主任史录文也曾表示,要真正让产品发挥作用,从招标、采购和整个医保报销、进入医院,都需要构建相应的配套机制。