业绩难以突破 研发实力不足 珍宝岛药业进军生物药领域 能否弯道超车?
来源:药智网 记者:时生
6月15日晚间,珍宝岛发布企业公告,拟与公司持股5%以上股东虎林龙鹏投资中心共同投资生物药企业浙江特瑞思药业股份有限公司。其中,珍宝岛拟出资4亿元,占特瑞思增资扩股后总股本的16.67%;龙鹏投资将其对特瑞思享有的6.2亿元债权转换为股权,占特瑞思增资扩股后总股本的25.84%。
业绩难以突破
加大研发,创新转型谋发展
珍宝岛药业属于中医药企业,医药政策的改革,医药市场逐渐收紧的大环境下,近年来,珍宝岛业绩尽管一直有稳中向上的趋势,但一直没有大的突破,据企业公告显示,2020年企业营业收入34.03亿元,同比增长仅3.4%。
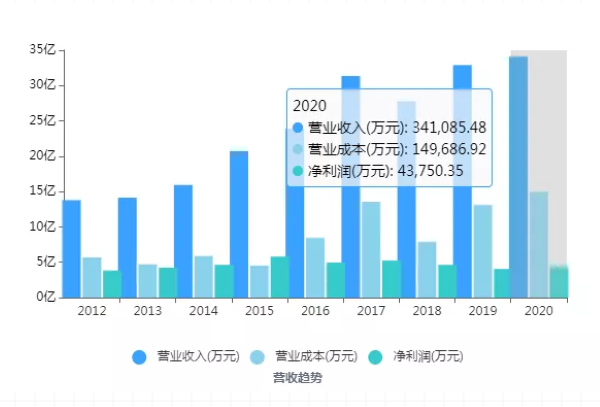
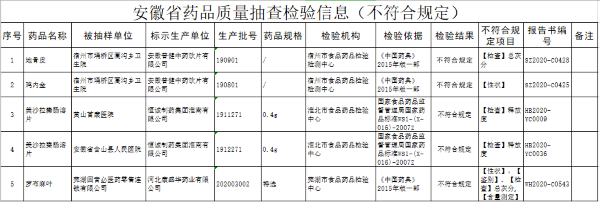
值得注意的是,其主营业务产品生物制剂与化学制剂的营业收入2020年更是大幅减少;其中生物制剂营业收入较上年下降55.18%,且其核心产品注射用骨肽2020年从国家医保目录剔除,销量仅为724.81万支,同比下降52.71%。
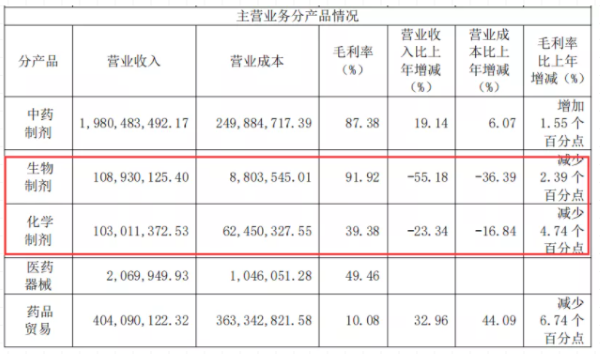
此外,据财报及行业分析,珍宝岛药业近年来虽然医药商业及药材销售业务获得了明显的扩张,但因为这部分业务的扩张,企业的净利率持续下降,再加上医药工业业务收入规模、获利能力均没有获得明显的增长,珍宝岛目前难以获得具有突破更好的业绩表现。
在目前的医药大环境下,想要具有突破性的业绩表现,研发出具有核心竞争力的创新产品是关键,才能在医药市场上才具备更高的话语权,而这便要追究企业的研发实力。
但从过去表现来看,珍宝岛的研发实力不足。据药智数据显示,截至目前珍宝岛药业累计仅4款1类创新药申报临床,其中HZB0071自2018年获批临床后,仍然处于临床批件阶段。
此外,除2020年外,此前珍宝岛每年研发投入不足1亿,研发投入占比不足营收的5%。
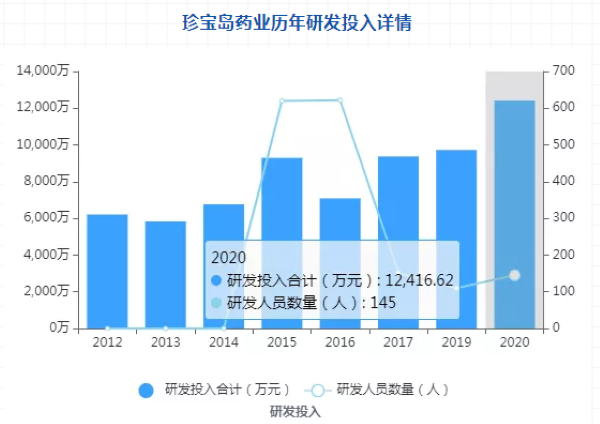
不过,据公告显示,珍宝岛药业将不断加大研发投入,坚持每年投入销售额3%左右的研发资金,据统计2020年研发投入已达1.2亿元,拥有研发人员145人。且一直在谋求创新转型,在立足于其具有优势的中药基础上,快速向化药和生物药领域拓展。
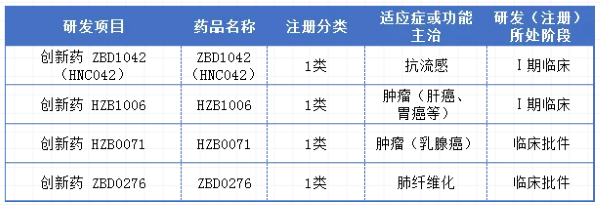
据悉,目前珍宝岛药业在研化药原料药有14个,化学制剂产品58个,1类创新药3个,两项获批临床,1项贮备申报IND。值得提及的珍宝岛药业通过自主研发、外部已经,已经初步构建了小分子创新药管线,目前共有4个创新药项目取得临床批件,包括2个抗肿瘤新药、1个抗流感新药和1个抗特发性肺纤维化新药。
抗肿瘤1类创新药物AKT激酶抑制剂HZB0071、抗肝癌1类创新药物pan-FGFR抑制剂HZB1006、抗流感病毒1类新药注射用HNC042、抗特发性肺纤维化1类新药ZBD0276片等创新药项目陆续获批并获得欧美专利。
强强联合,进军生物创新药领域
实现战略转型,接轨国际化
近年来,珍宝岛积极与国内顶尖的生物药研发团队深入沟通交流,探索生物药研发的多种合作模式,此次,珍宝岛药业斥资4亿元投资特瑞思,就是最好的行动证明。
据公告显示,特瑞思是一家集研发和商业化生产为一体的创新生物制药企业,拥有国际一流水平的CMC团队,能够生产高表达、高稳定性的细胞株。产品技术领域涉及靶向治疗、单抗偶联(ADC)、癌症的免疫治疗、双特异性抗体、纳米抗体等。
据官网信息,目前特瑞思有11个在研创新药和生物类似药产品,3个产品获批临床(I/III期)。其中特瑞思的贝伐珠单抗类似药TRS003、曲妥珠单抗生物类似药TRS004和创新型ADC药物TRS005有望未来2至3年将在美国及中国申报上市。
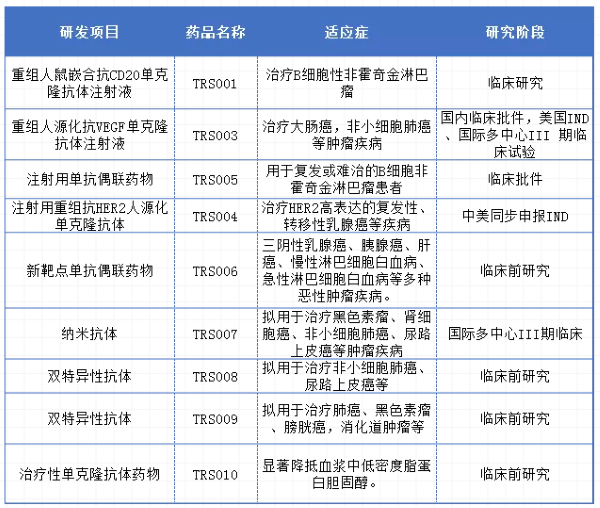
TRS003为贝伐珠单抗(商品名:安维汀®)的生物类似药。由于其高度类似的属性,是全球第一个被美国FDA批准做可互换III期临床试验的生物类似药,并且同意70%的患者来自于中国(全球首例)。现正在开展国际多中心III期临床试验,计划于2022年美国申报上市。
TRS004为曲妥珠单抗生物类似药,已获批美国临床,准备启动I期临床试验,计划于2023年美国申报上市。
TRS005为特瑞思自主研发的抗体偶联药物,目前在全球的研发进展处于领先地位,公告显示,由于其在临床阶段针对复发耐药非霍奇金淋巴瘤晚期病人的治疗显出了良好的疗效,今年8月将扩展为II期临床,II完成后申报有条件上市,计划于2022年中国申报上市,有望成为第一个上市的抗CD20-ADC产品。
截至目前,珍宝岛药业创新药暂无生物药在研,此次与特瑞思的合作无疑是宣告了珍宝岛准备进军生物创新药领域的决心,向着中药、化药、生物药“三足鼎立、全面出新”的研发理念发展;增强其公司的核心竞争力,能否在竞争激烈的国际生物药研发赛道上进行弯道超车,实现业绩突破性成长,拭目以待。