未来相关药企的竞争可能更加激烈
相关品种尚未通过仿制药质量和疗效一致性评价的企业终于等到关于评价时限的最新要求。日前,国家药品监督管理局发布了《关于仿制药质量和疗效一致性评价有关事项的公告》(简称“公告”)及相关政策解读,明确表示,“时间服从质量,合理调整相关工作时限和要求”,这意味着“289基药目录”仿制药一致性评价2018年12月31日大限取消。不过,这并不意味着一致性评价可以无限延期,相反,未来相关药企的竞争可能更加激烈,某种程度上会倒逼药企发展高质量仿制药。
公告指出,《国家基本药物目录(2018年版)》(简称“新版目录”)已于2018年11月1日起施行,新版目录建立了动态调整机制,对通过一致性评价的品种优先纳入目录,未通过一致性评价的品种将逐步被调出目录。充分考虑基本药物保障临床需求的重要性,对纳入国家基本药物目录的品种,不再统一设置基本药物评价时限要求。
不再统一设置基本药物评价时限要求,不等于没有时限要求。公告表示,化学药品新注册分类实施前批准上市的含基本药物品种在内的仿制药,自首家品种通过一致性评价后,其他药品生产企业的相同品种原则上应在3年内完成一致性评价。逾期未完成的,企业经评估认为属于临床必需、市场短缺品种的,可向所在地省级药品监管部门提出延期评价申请,经省级药品监管部门会同卫生行政部门组织研究认定后,可予适当延期。
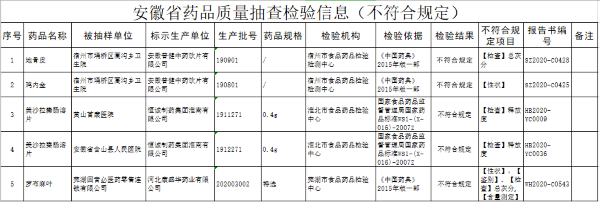
据GBI SOURCE数据库显示,截至2018年12月28日,药品评审中心有关一致性评价累计受理号已达708个,涉及253家企业的205个品种。目前,已有149个品规通过或视同通过仿制药一致性评价,62个品规包含在289目录,涉及32个品种。其中,1个品规通过企业有5家,3个品规通过企业有4家,6个品规通过企业有3家,14个品规通过企业有2家,86个品规通过企业有1家。
鼓励高品质仿制药的发展可以节省大量的医保基金支出,既符合国际发展趋势,又是供给侧改革的重要手段。业内专家对上证报记者说,两类药将更具市场前景:一是通过仿制药质量和疗效一致性评价的市场急需的大品种;二是按照原研药质量和疗效一致快速仿制即将到期的专利畅销药。
据统计,国内已通过一致性评价的品种中,有多个品种的原研厂家全球销售峰值在40亿美元以上,如阿托伐他汀、氯吡格雷、恩替卡韦、喹硫平、阿卡波糖、瑞舒伐他汀、奥氮平、孟鲁司特等。这些品种在国内市场规模大多在20亿元以上,并且进口/原研厂家的份额大多在三成以上,有的高达七成以上,这些品种的进口替代空间最大。目前已通过一致性评价的品类中,瑞舒伐他汀已有正大天晴、海正药业、京新药业、先声药业等四家企业通过;恩替卡韦已有正大天晴、海思科、江西青峰药业等3家企业通过。
引人关注的是,2017年至2029年至少有24个重磅药品专利到期,但目前在国内尚无企业进行抢仿申报。